1. ¿Por qué se
llama al Citoplasma “Encrucijada de Vías Metabólicas”?
Debido a que es
el lugar donde se cruzan dos o más vías metabólicas en las cuales se desarrollan
grandes cantidades de reacciones bioquímicas, reacciones de degradación del
catabolismo y anabolismo que se realizan simultáneamente y que conciernen al
metabolismo de los glucósidos, los nucleósidos, los ácidos grasos y de los
aminoácidos.
2. Clasifica los
materiales que conforman el hialoplasma
Ø Según sus propiedades físicas: se describe como un
líquido semitransparente elástico que contiene partículas suspendidas y una
serie de minúsculos túbulos y filamentos que forman un citoesqueleto.
Ø Según sus propiedades químicas: es 75% a 90% agua.
3. Diagrama La Vía
de las Pentosas.
4. Respecto a la Glucólisis indica: etapas en
las que se invierte ATP, etapas en la que se genera ATP (a nivel de substrato),
Coenzimas reducidas a ser “cobradas” o reoxidadas. En todos los casos indica la
enzima.
5. Explica el
papel de la Aldolasa y la isomerasa en la Glucólisis.
|
Aldolasa.
|
Isomerasa.
|
|
Cataliza la escisión
de la fructosa-1,6-bisfosfato en dos triosas, dihidroxiacetona fosfato y gliceraldehído
3-fosfato.
|
Adiciona grupo
fosfato a la glucosa, su conversión en fructosa y la adición de otros grupos
fosfato a la fructosa.
Transforma la dehidroxiacetona a
gliceraldehido 3 fosfato.
|
6. Diagrama el
destino del Piruvato en condición a) Anaerobica y b) Aeróbica.
7. Explica los
dos posibles orígenes de la Coenzima A.
Beta oxidación
de los ácidos grasos: Las enzimas
remueven dos átomos de carbonos por vez de una larga cadena de átomos de
carbono que componen a un ácido graso y unen el fragmento de dos carbonos
llamado grupo acetilo a la Coenzima A para formar Acetil Coenzima A molécula
que puede ingresar en el ciclo de Krebs, otro de los resultados es que dichas
reacciones generan coenzimas reducidas (NADH y FADH2) que pueden ingresar en la
cadena respiratoria.
Descarboxilación
oxidativa del ácido pirúvico. Cada molécula de
piruvato producida en la glucolisis se transporta a través de la membrana
mitocondrial interna y hacia la matriz, donde se descarboxila para formar un
grupo acetilo de dos carbonos, esta etapa de transición ocurre entre la glucosa
y el ciclo de Krebs. Este fragmento de dos carbonos, se une a la CoA y se forma
Acetil-CoA, en donde durante esta reacción el NAD+ oxidado es reducido NADH+ + H+, catalizado por reacción del complejo enzimático
deshidrogenasa de piruvato. Una vez cumplido el proceso la CoA, se encuentra
preparada para incorporarse al ciclo de Krebs. Esta reacción es imprescindible
para que la oxidación de los glúcidos continúe por la vía aerobia (ciclo de
Krebs, cadena respiratoria, fosforilación oxidativa). De este modo puede
aprovecharse toda la energía contenida en dichos nutrientes, con obtención de
una cantidad máxima de ATP.
9. Compara la
cadena de Transporte de electrones (indicando cada transportador) con las Bombas
de Protones (indicando cada transportador). Destaca la entrada de cada coenzima
reducida (NADH Y FADH) en el determinado transportador. Sigue la ruta de la Fuerza protón Motriz hasta la ATP
sintetasa hasta la Síntesis de ATP.
La cadena transportadora de electrones consiste
en 4 complejos de portadores de electrones y dos portadores mas (ubiquinona y
citocromo) que se disponen de manera independiente.
Los electrones entran en la cadena a partir de NADH mediante el complejo I y
cataliza la transferencia de un par de electrones de NADH a la ubiquinona (UQ)
generalmente por medio del centro FeS de complejo I.
En el complejo
III (citocromo BCl) se cataliza la transferencia de electrones del ubiquinona
al citocromo c, a su vez los protones son bombeados al espacio intramembranoso.
El complejo IV
(oxidasa de citocromo) se cataliza la reducción de O2. Por cada
molecula de O2
reducida por la oxidasa de citocromo se captan 8 protones, 4 de ellos se consumen
en la formación de dos moléculas de agua, los otros cuatro son liberados al espacio
membranoso.
Los protones que son bombardeados a través de la
membrana mitocondrial interna, genera que el gradiente de protones sea mayor en
la matriz, por lo que por medio de esto puede ser utilizado a fin de
suministrar la energía para síntesis de ATP mediante la fosforilación del ATP.
10. Compara la
Glucogénesis con la Glucogenólisis.
|
Glucogénesis
|
Glucogenolisis
|
|
Ruta anabólica
por la que tiene lugar la síntesis de glucógeno a partir de un precursor más
simple, la glucosa-6-fosfato. Se lleva a cabo principalmente en el hígado, y
en menor
medida en el músculo, es activado por insulina en respuesta a los altos niveles
de glucosa, que pueden ser posteriores a la ingesta de alimentos con carbohidratos
|
Proceso catabólico
llevado a cabo en el citosol que consiste en la remoción de un
monómero de
glucosa de una molécula de glucógeno mediante fosforilación para producir
glucosa 1 fosfato, que después se convertirá en glucosa 6 fosfato, intermediario
de la glucólisis.
|
11. Describe brevemente la GlucoNeoGénesis.
Es una ruta metabólica
anabólica que permite la síntesis de glucosa a partir de precursores no
glucídicos. Incluye la utilización de varios aminoácidos, lactato, piruvato,
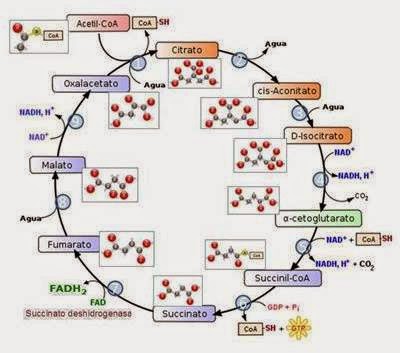
glicerol y cualquiera de los intermediarios del ciclo de los ácidos
tricarboxílicos o CICLO de Krebs como fuentes de carbono para la vía
metabólica. Todos los aminoácidos, excepto la leucina y la lisina, pueden
suministrar carbono para la síntesis de glucosa.
12. A que se llama Ciclo de Cori.
A la circulación
cíclica de la glucosa y el lactato entre el músculo y
el hígado. Las células musculares se alimentan principalmente de glucosa
de sus reservas glucogénicas y sobre todo de la que llega a través de
la circulación sanguínea procedente del hígado. A lo largo del
ciclo, el glicógeno muscular es desglosado en glucosa y
ésta es transformada a piruvato mediante la glucólisis. Este piruvato se transformará en lactato por la vía del
metabolismo anaeróbico gracias a la enzima lactato deshidrogenasa. El lactato es
transportado hasta el hígado por vía sanguínea y allí es reconvertido a
piruvato, y, después, a glucosa a través de la gluconeogénesis. La glucosa
puede volver al músculo para servir como fuente de energía inmediata o ser
almacenado en forma de glucógeno en el hígado.





.jpg)













.jpg)


.jpg)